Строение Атома Химия Презентация
Слайды и текст этой презентации. Строение атома. Строение атома Опыт Эрнеста Резерфорда Модель строения атома Элементарный состав атома Характеристика частиц, входящих в состав атома Фундаментальные законы микромира. Опыты Резерфорда (без фольги) 3. Презентация 8 класса по предмету 'Химия' на тему: 'СТРОЕНИЕ АТОМА Урок по химии в 8 классе по учебнику О.С. Габриеляна учителя химии МБОУ.
Универсальный пульт ДУ. 2-в-1 для ТВ/DVD SRU1020/10 Найти похожие продукты. Универсальный пульт ДУ. Обзор Характеристики Отзывы. Philips(Филипс, филлипс) SRU1060/10 Пульт Ду Универсальный, инструкция, поддержка, форум, описание, мануал, руководство, форум, Инструкция по эксплуатации. По эксплуатации. 15, pdf, 1.24MB. Загрузить Просмотр. Руководства пользователя и инструкции по эксплуатации Philips SRU1060/10 помогут настроить устройство, найти ошибки и исправить неполадки. Philips sru 1060 инструкция pdf. Инструкция Philips SRU-1060. Русская инструкция по эксплуатации. Универсальный пульт ДУ. Размер файла (кБ): 1298. Цена: 100.00 руб. Philips Universal remote control SRU1060 2in1 for TV/DVD. Брошюра Version:3.0, PDF файл, 323.5 kB, опубликовано 10 декабря 2007 г.
Химия 8 класс краткое содержание других презентаций - 1 моль хлора. Особая единица.

Как и в каких единицах можно измерить вещество. Заполняем таблицы. В порции вещества содержится 6 1023 молекул. Молярная масса.
Число частиц. Постоянная Авогадро. Рабочая тетрадь с печатной основой. Количество вещества.
Определите число молекул. Предисловие. Молярная концентрация растворов. Какова массовая доля сахарозы в полученном растворе. Определите массовую долю кислоты в полученном растворе. Растворимость бертолетовой соли.
Разбавление растворов. Задачи, связанные со смешиванием растворов. Задачи на тему растворы из ЕГЭ 2012.
Действия с растворами. Рассчитайте массовую долю кристаллогидрата. В какой массе воды нужно растворить 125 г медного купороса. Классификация кислот по строению кислотного остатка. Взаимодействие кислот с основаниями. Разложение кислот. Бескислородные HF, H Cl, H Br, HI H2S.
Физические свойства. Некоторые кислоты разлагаются при н.у. Или при нагревании: Соль + кислота = новая соль + новая кислота. Что такое кислоты? NaOH Фенол- фталеин. Твёрдые вещества, растворимые в воде: H3PO4, HPO3 Нерастворимая в воде H2SiO3. Жидкости, неограниченно смешивающиеся с водой: H2SO4, HNO3, HCI и др.
Местоположение химических элементов. Авторы славянской письменности. Географические начала. Назовите «координаты» элементов. Структура периодической системы.
Обозначения химических элементов. Алхимические символы элементов.
Происхождение названий химических элементов. Игра «Координаты». Свойства простых веществ. М.В.Ломоносов в химии. Элементы математической химии. Научный труд Ломоносова.
Химическая лаборатория. Всеобщий закон природы. Welcome 3 teacher`s book. Технология цветных стёкол. Ломоносов умирает от случайной простуды. Весовой анализ. Лаборатория Ломоносова. Физическая химия.
Первые русские академики. Теория растворов. Научные достижения М.В.
Ломоносова в химии. Первая химическая лаборатория. Допиши химические реакции. Природный газ. Получение водорода в промышленности. Карта с космоса. Производство минеральных удобрений.
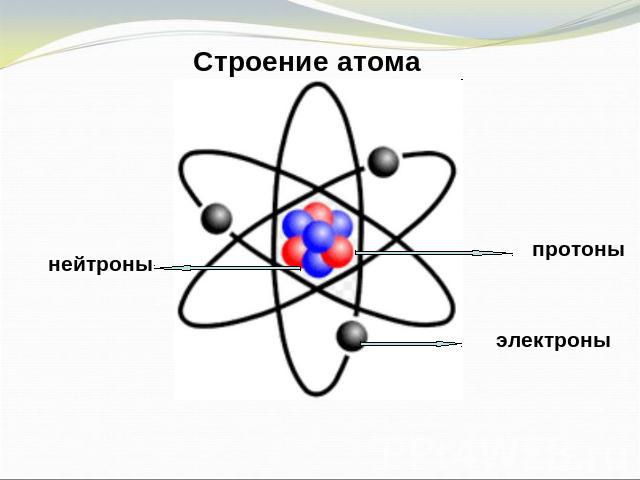
Строение Атома Лития
Получение водорода в промышленности и его применение. Применение водорода. Способы получения.
Строение Атома Химия Презентация
Типы реакций. Способы получения водорода. Всего в теме 53 презентации.